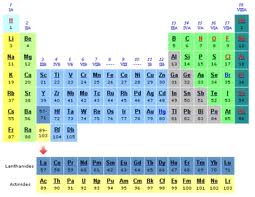
Mendeleev é autor da lei segundo a qual as propriedades físicas e químicas dos elementos são função periódica do peso atômico. Apesar de outros cientistas terem anteriormente traçado seqüências numéricas entre os pesos atômicos de certos elementos e notado conexões entre estes e as propriedades das diversas substâncias, Mendeleev é o primeiro a enunciar a lei cientificamente.
 Estabelece a analogia dos elementos em bases numéricas seguras. Faz a classificação periódica dos elementos químicos conforme seu peso específico, dispondo os elementos em ordem crescente de acordo com seu peso atômico. Nota que as propriedades dos corpos simples se repetem periodicamente. Elabora quadros que, por apresentarem lacunas, o levam a prever a existência três elementos até então desconhecidos, previsão confirmada pela descoberta do gálio (1875), do escândio (1879) e do germânio (1886). Em diversos casos questiona os pesos atômicos aceitos por não corresponderem à lei periódica.
Estabelece a analogia dos elementos em bases numéricas seguras. Faz a classificação periódica dos elementos químicos conforme seu peso específico, dispondo os elementos em ordem crescente de acordo com seu peso atômico. Nota que as propriedades dos corpos simples se repetem periodicamente. Elabora quadros que, por apresentarem lacunas, o levam a prever a existência três elementos até então desconhecidos, previsão confirmada pela descoberta do gálio (1875), do escândio (1879) e do germânio (1886). Em diversos casos questiona os pesos atômicos aceitos por não corresponderem à lei periódica.Mendeleev empreende trabalhos sobre o isomorfismo, a compressão dos gases e as propriedades do ar rarefeito. Estuda a natureza das soluções, que considera sistemas líquidos homogêneos de compostos instáveis dissociáveis do solvente com a substância dissolvida. Investiga a expansão termal dos líquidos e elabora fórmula para expressá-la. Estudando os gases (1861) antecipa o conceito de Thomas Andrews (1869) da temperatura crítica dos gases, definindo o ponto absoluto de ebulição como a temperatura em que a coesão e o calor da vaporização eqüivalem a zero e o líquido se transforma em vapor independentemente da pressão e do volume. Contribui ainda para a preparação de uma pólvora sem fumaça, à base de pirocolódio. Sua obra mais importante é Osnovy chimii (1868 – 1870; Princípios de química).